Osteologie 2010 (Osteoporose)
In Berlin hat im März das internationale Meeting "Osteologie 2010" stattgefunden. Dieser Bericht fokussiert auf die SERM-Therapie für physiologischen Knochenaufbau. Internationale und Schweizer Experten standen Red und Antwort zum Thema.
 |
|
Osteologie 2010 - Berlin | |
| |
SERM-Therapie für physiologischen Knochenaufbau
Frakturprävention besonders in Frühstadien der Osteoporose wirksam
Der Selektive Östrogenrezeptor-Modulator (SERM) Raloxifen gehört zu den mit höchster wissenschaftlicher Evidenz für die Therapie der postmenopausalen Osteoporose zugelassenen Medikamenten. Die selektive Wir kung von Raloxifen (Evista®) führt zum Aufbau eines physiologisch wertvollen Knochens, was bereits ab einem T-Score von -1 nutzbar ist. An anderen Geweben wie dem Endometrium und der Brustdrüse hingegen kommt es nicht zur Proliferation. Durch dieses pharmakologische Prinzip wird gleichzeitig das Risiko des invasiven Mamma-Karzinoms vermindert. Diese Erkenntnisse wurden auf dem wissenschaftlichen Symposium SERM-Therapie der Osteoporose Knochenstabilität durch Qualität anlässlich des Kongresses Osteologie 2010 am 4. März 2010 in Berlin vermittelt.
Target-Therapie der Osteoporose
Über die Östrogenrezeptoren wird bei gesunden, prämenopausalen Frauen der Knochenstoffwechsel massgeblich gesteuert. Daher ist dieses Target für die Therapie der postmenopausalen Osteoporose, bei der ein Östrogenmangel prädominant ist, von grosser Bedeutung. Das betonte Prof. Dr. Lorenz Hofbauer von der Abt. Endokrinologie, Diabetologie und Osteologie an der Med. Klinik III am Universitätsklinikum der TU Dresden. Der Östrogenrezeptor ist quasi der Gatekeeper der Frauengesundheit. Über ihn wird auch die mentale Gesundheit, die Straffheit der Haut sowie die Funktion des Gefässsystems gesteuert.
Physiologische SERM-Wirkungen
Selektive Östrogenrezeptor-Modulatoren (SERM) sind keine Östrogene, Gestagene oder irgendwelche andere Hormone. Sie binden jedoch an die Östrogenrezeptoren (ER), die sie in unterschiedlicher Weise und je nach Gewebe differenziert zu modulieren vermögen. Im Falle des einzigen für die Osteoporose- Therapie verfügbaren SERM Raloxifen ist die Wirkung am Knochen Östrogen-ähnlich, während an anderen Geweben wie z.B. dem Endometrium oder Brustgewebe eine Anti-Östrogen-Wirkung zu beobachten ist. Im Brustgewebe hat Raloxifen antiproliferatorische Wirkungen.
Einfluss auf den Knochenstoffwechsel
Der SERM Raloxifen beeinflusst den Knochenstoffwechsel nicht nur über den Östrogenrezeptor, sondern auch über das RANKLOsteoprotegerin- System, wie Prof. Hofbauer erläuterte (Viereck V et al. J Clin Endocrinol Metab. 2003;88:4206-13). In einer soeben im New England Journal of Medicine erschienenen Übersichtsarbeit über die Wirkung von SERM (Becker C N Engl J Med 2010; 362:752-4) wird nochmals zusammengefasst, was Raloxifen für die Gesundheit von Frauen in der Postmenopause bewirkt:
- Prävention von vertebralen Frakturen (-68% im 1. Jahr),
- Zuwachs der Knochensubstanz (BMD nach DXA): 2,7% im Bereich der lumbalen Wirbelkörper, 2,4% am proximalen Femur,
- Prävention des ER-positiven Mammakarzinoms (-90%),
- Endometrium-Hyperplasie oder -Karzinom: kein Effekt.
Angesichts dieser theoretischen und klinischen Daten ist es, so Prof. Hofbauer abschliessend, unverständlich, warum ein Medikament mit einem so breiten Einfluss auf die Gesundheit der postmenopausalen Frau nicht häufiger eingesetzt wird.
Knochenqualität erlaubt Antwort auf unterschiedliche Belastungen
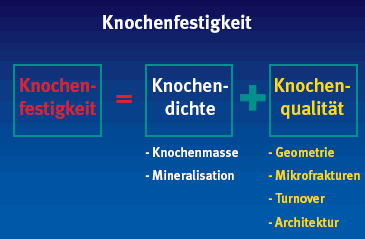
Wie Univ. Doz. Dr. Astrid Fahrleitner-Pammer, von der Klin. Abt. für Endokrinologie & Nuklearmedizin der Med. Universität Graz (Österreich) ausführte, steht bei der Osteoporose-Therapie bisweilen nur der Aufbau der starren Festigkeit des Knochens im Vordergrund. Das reicht jedoch nicht. Denn ohne seine elastischen Eigenschaften fehlt dem Knochen die Biegsamkeit und er ist vielen alltäglichen Belastungen nicht gewachsen. Wie Abb. 1 zeigt, wird die Knochenstärke, nach der sich die Belastbarkeit richtet, sowohl durch die Knochendichte (Knochenmasse und -mineralisation, mess - bar in DXA) als auch durch die Knochenqualität bestimmt, die durch die Geometrie, die Zahl der Mikrofrakturen, den Knochenumbau und die Architektur bestimmt wird.
 |
|
Abbildung 1: Faktoren, die zur Belastbarkeit des Knochens beitragen (Modifiziert nach Fahrleitner-Pammer A 2010) | |
| |
Je nach Lokalisation sind die Anforderungen und daher auch die Strukturen des Knochens unterschiedlich. Die Belastbarkeit des Knochens durch äussere Einwirkungen (Stress) nimmt nur bis zu einer Knochenmasse von 66% zu, um dann drastisch abzunehmen (Abb. 2). Bei solchen Patienten gaukeln zunehmende Bone-Mineral-Densitiy-(BMD-)Werte aus der DXA-Messung Arzt und Patienten eine Sicherheit vor, die nicht gegeben ist.
 |
|
Abbildung 2: Knochenmasse und Belastbarkeit (Modifiziert nach Fahrleitner-Pammer A 2010) | |
| |
Inzwischen gelang es, in einer schweizerisch- deutschen Studie nachzuweisen, dass unter Raloxifen die Knochenqualität zunimmt (siehe Kasten):
| Dokumentierte Verbesserung der Knochenqualität unter Raloxifen |
|
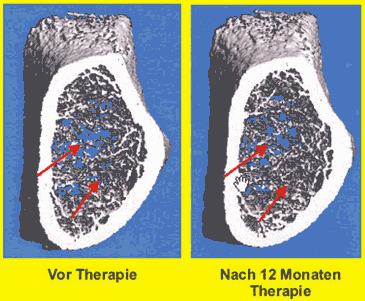
Seit Mitte 2008 wird in einer prospektiven Beobachtungsstudie in München und Zürich überprüft, ob sich unter der Therapie mit Raloxifen bei Patientinnen mit Osteopenie oder Osteoporose die volumetrische trabekuläre bzw. kortikale Knochendichte (vBMD) sowie die quantitative und qualitative Mikroarchitektur verbessert. Das von Radspieler H, Dambacher MA und Neff M vorgestellte Poster Raloxifen und Knochenqualität eine prospektive Anwendungsbeobachtung (Osteologie 2010, Poster OP3.7/P24) zeigt sowohl im Bereich des Radius wie auch der Tibia in den Parametern Gesamtdichte vBMD, trabekuläre Dichte, innere trabekuläre Dichte, kortikale Dichte, trabekuläres Knochenvolumen, Trabekelzahl, mittl. Trabekelabstände und Kortikalisdichte bereits nach im Schnitt 15.1 Monaten Zuwächse zwischen 0.5 und 6.2%. Lediglich beim Messwert mittl. Trabekeldicke fielen die Werte ab. Die Messungen erfolgten mittels HRpQCT. Bei einigen Patientinnen zeigten sich bereits sichtbare Verbesserungen der 3D-Mikroarchitektur (Abb. 3). Die positiven Veränderungen der Strukturparameter sprechen für einen Zuwachs der Knochenqualität unter Raloxifen (Evista®).
 |
|
Abbildung 3: Zunahme der Trabekelanzahl am ultradistalen Radius einer Patientin vor und nach 12 Monaten Therapie mit Raloxifen (Radspieler H et al. Osteologie 2010, Poster OP3.7/P24)
| |
| | |
Leistungsspektrum von Raloxifen
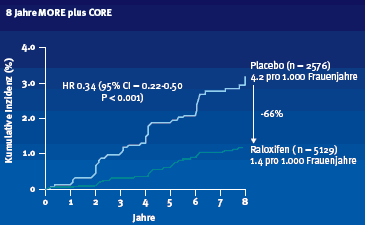
Evista® (Raloxifen) ist der am besten evaluierte SERM in der Osteoporose Therapie. Als einziges Präparat dieser Klasse ist es für die Prävention und Therapie der postmenopausalen Osteoporose zugelassen. In den grossen prospektiven Studien MORE, CORE, RUTH und STAR wurden insgesamt fast 40'000 Patientinnen eingeschlossen. Geprüft wurde die Wirksamkeit bei Patientinnen mit postmenopausaler Osteoporose, mit erhöhtem koronaren Risiko oder erhöhtem Risiko für ein Mammakarzinom. Prof. Dr. Kurt Lippuner von der Universitätspoliklinik für Osteoporose am Inselspital Bern (Schweiz) resümierte anhand dieser Studien das Nutzen/Risikoprofil von Raloxifen. Die wichtigste Studie zum Nachweis der Eignung von Raloxifen zur Fraktur-Prävention in der Post-Menopause war die Multiple Outcomes of Raloxifene Evaluation-(MORE-) Studie an 7'705 Patientinnen. Hier fand sich in der Gruppe mit vorbestehenden Frakturen unter 60 mg Raloxifen pro Tag nach 3 Jahren eine Verminderung radiologisch nachgewiesener vertebraler Frakturen um 30% im Vergleich zu Plazebo (RR 0.7). Bei Patientinnen ohne vorbestehende Frakturen fand sich eine Verminderung der vertebralen Frakturen um 50%. Eine Verminderung des Risikos neuer vertebraler Frakturen um 47% liess sich auch bei osteopenischen Frauen zeigen. Ein signifikanter Rückgang des Risikos nicht-vertebraler Frakturen liess sich in einer posthoc-Analyse der MORE-Studie nur bei Patientinnen mit vorbestehenden schweren Frakturen nachweisen. Die MORE-Studie wurde unter dem Akronym CORE (Continuing Outcomes Relevant to Evista®) für vier Jahre weitergeführt. Die vorliegenden 7-Jahres-Daten aus dem MORE-CORE-Kollektiv zeigen eine über die gesamte Studie anhaltende Verbesserung der BMD-Werte im Lumbal- und proximalen Femur- Bereich. Schon in der MORE-Studie war ein Rückgang der Häufigkeit von Mamma-Karzinomen nachweisbar (3,6/1.000 Patientenjahre unter Plazebo auf 0,9/1.000 Patientenjahre unter Raloxifen). Die Risikoreduktion betrug 76%. Nimmt man die Daten der CORE- Studie über insgesamt 8 Jahre hinzu (n=4.011), so zeigt sich eine Reduktion des Risikos für ein invasives Mamma-Ca von 66% (Abb. 4). Diese Daten sind, wie Prof. Lippuner erklärte, bislang für ein Produkt der Osteoporose Prophylaxe in der Prävention des Mamma-Ca einzigartig.
 |
|
Abbildung 4: Inzidenz des invasiven Mamma-Ca bei Osteoporose-Patientinnen in der MORE- und CORE-Studie (Modifiziert nach Martino S et al. J Natl Cancer Inst 2004; 96:1751-61) | |
| |
Insgesamt empfiehlt Prof. Lippuner Raloxifen (Evista®) bei allen Patientinnen mit gegebener Indikation zur Prävention osteoporotischer Frakturen möglichst früh einzusetzen. Die Therapie sollte möglichst schon dann ansetzen, wenn die grösste Chance besteht, die erste Fraktur zu verhindern, nämlich im osteopenischen Bereich (DXA T-Score =1). Diese Indikation ist in der Schweiz erstattungsfähig. Ein erhöhtes Brustkrebs-Risiko ist ein zusätzliches Argument, Raloxifen bei gegebener Osteoporose-Indikation anzuwenden.
Die Patientin sollte nicht am Beginn der Menopause stehen, kein bekanntes thromboembolisches Risiko haben und während einer temporären Erhöhung des Thromboserisikos, etwa durch eine Immobilisierung, die Therapie unterbrechen.
Experten Interviews
Interview mit Prof. Dr. med. Peyman Hadji
|
|
|
Prof. P. Hadji, Marburg |
 |
| |
Mit einem SERM auf der physiologischen Seite
Herr Prof. Hadji, sind Bisphosphonate in der Frakturprävention wirksamer als Raloxifen?
Hadji: Zwischen beiden Medikamentengruppen gibt es keine direkten Vergleichsstudien. Wenn ich z.B. in einem Kollektiv untersuche, das bereits ein bis zwei Frakturen erlitten hat, wie das in den meisten Bisphosphonatstudien der Fall war, wird die Wirksamkeit eindrucksvoller sein, als in einem Kollektiv, das noch keine Frakturen erlitten hatte. Von daher sind diese Vergleiche der relativen Risikoreduktionen irreführend und eher im Bereich des Pharmamarketings anzusiedeln. Wir haben zu fragen: Gibt es eine substantielle Risikoreduktion und wie gross ist die absolute Risikoreduktion in einem definierten Patientenkollektiv? In den DVO-Leitlinien von 2009 sind die Medikamente mit einem Wirkungsnachweis für die Prä - ven tion von Wirbel- bzw. Schenkelhalsfrakturen entsprechend A-klassifiziert. Für mich ist Raloxifen in der Reduktion von Wirbelkörper-Frakturen äquipotent zu Bisphosphonaten. Für eine Beurteilung der Reduktion nicht-vertebraler Frakturen war das Patientenkollektiv der MORE-Studie leider wenig geeignet. Aber auch aus pathophysiologischen Gründen kann ich mir nicht vorstellen, dass ein SERM an der Lendenwirbelsäule wirkt, das heisst signifikant vor Frakturen schützt, und am Schenkelhals nicht. Auch Östrogene zeigen eine klare Frakturreduktion am Schenkelhals und an der Wirbelsäule.
Nun wird im Zusammenhang mit SERMs von einem physiologischen Knochenaufbau gesprochen. Wie kann man das verstehen?
Hadji: Der Knochen einer prämenopausalen Frau, die ja normal östrogenisiert ist, stellt einen Idealzustand dar. Hier sehen wir eine normale Frakturheilung, einen normalen Knochenauf- und - abbau, also einen physiologischen Knochen. Dieser Zustand kommt in der Postmenopause durch Östrogenmangel aus dem Lot. Wir können das Ungleichgewicht durch eine Resorptionshemmung auszugleichen suchen. Aber Bisphosphonate schiessen quasi über das Ziel hinaus und supprimieren den Knochenstoffwechsel stärker, als wir es bei der prämenopausalen Frau sehen. Negative Effekte sind bisher nicht belegt, aber wir können uns fragen: Muss das überhaupt sein? Meiner Auffassung nach muss es nicht sein!
Wenn es uns z.B. mit einem SERM gelingt, den Knochenstoffwechsel in den physiologischen Bereich zurückzuführen, dann haben wir die Idealkonstellation wieder hergestellt. Das muss eine Therapie leisten, das leistet Raloxifen. Wenn Medikamente mehr leisten, muss das nicht immer gut sein...
Man hört auch, Raloxifen sei zu teuer für seinen Effekt...
Hadji: ...das richtet sich nach dem Wert der Sache. Raloxifen bietet einen Zu - satz effekt, der einen höheren Preis etwa im Vergleich zu generischem Alendronatrechtfertigt: Die Reduktion des invasiven, Rezeptor-positiven Mammakarzinoms. Das ist ein einzigartiger Zusatznutzen. Ob das nun die Kosten eines solchen Präparates rechtfertigt, muss letztlich die Patientin, der Arzt bzw. die Kasse oder die KV entscheiden. Ich denke, wir sollten wie auch in unseren Leitlinien erwähnt diesen Zusatznutzen immer im Auge haben.
Herr Prof. Hadji, recht herzlichen Dank für das Gespräch!
Interview mit Prof. Dr. med. Kurt Lippuner
|
|
|
Prof. K. Lippuner, Bern |
 |
| |
Frühzeitige Gabe von Raloxifen erspart Gesundheitskosten
Herr Prof. Lippuner, in der Therapie der postmenopausalen Osteoporose wird der beste Zeitpunkt für den Beginn einer Frakturprävention diskutiert. Ab wann sollte man Frauen mit Medikamenten wie Raloxifen versorgen?
Lippuner: Die Daten für Raloxifen belegen, dass man dieses Medikament bereits frühzeitig einsetzen kann. Wir geben es bei Frauen, die eine verminderte Knochendichte (i.S. einer Osteopenie) mit erhöhtem Frakturrisiko haben. Damit gelingt es uns, wie auch in einigen Studien gezeigt werden konnte, die erste Fraktur zu verhindern. Das ist unser wichtigstes Therapieziel: Die Frauen zu behandeln, bevor sie an den Folgen von Wirbelfrakturen zu leiden haben.
Nun wird gerade in Deutschland und vor allem von den Kassen argumentiert, dass diese Frauen noch nicht richtig krank seien. Was würden Sie darauf antworten?
Lippuner: Ja, das ist natürlich eine sehr kurzfristige Optik, wenn man darauf wartet, bis durch Frakturen massive Gesundheitskosten entstehen. Wir haben in der Schweiz auch zeigen können, dass die Osteoporose einer der Haupt-Kostentreiber im Gesundheitswesen ist. Das wird auch in Deutschland nicht anders sein.
Ausserdem gibt es gerade für Raloxifen Studien, die eine Kosteneffizienz seines frühzeitigen Einsatzes belegen. Das wird nicht nur durch die Prävention osteoporotisch bedingter Frakturen bedingt, sondern auch durch die Verminderung des Brustkrebs-Risikos unter dieser Therapie.
Abgesehen einmal von den DXA-Werten, mit denen Sie eine Osteopenie diagnostizieren, welche Patientinnen sehen Sie bevorzugt unter der Therapie mit Raloxifen?
Lippuner: Sicherlich Frauen mit Risikofaktoren für Frakturen und einer verminderten Knochendichte, die sich nicht am Beginn der Menopause befinden, also nicht mehr an starken Wallungen leiden. Das kann also eine Frau im Alter ab 55 Jahren bis 75 Jahre sein. Die älteren Frauen sind dann mehr durch Schenkelhalsfrakturen gefährdet. Da müsste dann ein Medikament eingesetzt werden, dass speziell auch Hüftfrakturen verhindert. Wenn nebst dem erhöhten Wirbelfrakturrisiko auch noch ein erhöhtes Risiko für ein Mammakarzinom gegeben ist, spricht dies umso mehr für einen Einsatz von Raloxifen.
Herr Prof. Lippuner, recht herzlichen Dank für das Gespräch!
Bericht und Interviews von Dr. rer. nat. Till U. Keil, München
Kongress Osteologie 2010"
30.06.2010 - dde
Mit freundlicher Unterstützung von Daiichi Sankyo